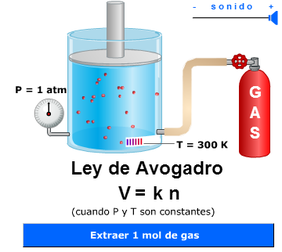
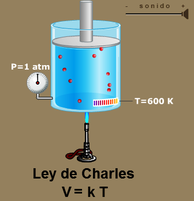
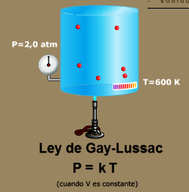
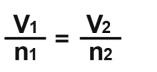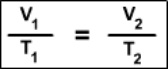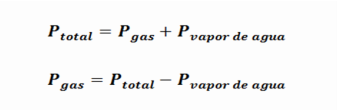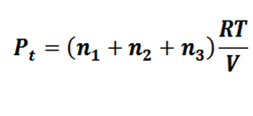En estado gaseoso las partículas son independientes unas de otras, están separadas por enormes distancias con relación a su tamaño. Tal es así, que en las mismas condiciones de presión y temperatura, el volumen de un gas no depende más que del número de partículas (Ley de Avogadro) y no del tamaño de éstas, despreciable frente a sus distancias.
Medidas en los gases:
Para definir el estado de un gas se necesita cuatro magnitudes: masa (cantidad de gas), presión, volumen y temperatura. Por lo tanto, las leyes de los gases toman el estudio del volumen (V) en función de la presión (P), temperatura (T) y cantidad de gas (n).
Ley o principio de Avogadro
|
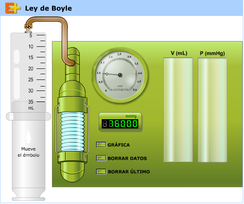
Ley de Boyle
|
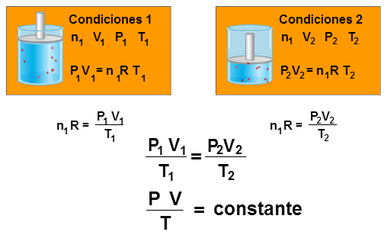
LEY COMBINADA DE LOS GASES
Esta ley relaciona el volumen, la presión y la temperatura, teniendo la cantidad de gas constante.
La ley se enuncia así: “Para una masa determinada de cualquier gas, se cumple que el producto de la presión por el volumen dividido entre el valor de la temperatura es una constante”. Donde las temperaturas se expresan en kelvin.
La formula se enuncia así:
La ley se enuncia así: “Para una masa determinada de cualquier gas, se cumple que el producto de la presión por el volumen dividido entre el valor de la temperatura es una constante”. Donde las temperaturas se expresan en kelvin.
La formula se enuncia así:
Da clic sobre la imagen para ver la simulación de esta ley:
LEY DE LOS GASES IDEALES O ECUACIÓN DE ESTADO
|
Esta ley relaciona las leyes de Boyle, Charles y el principio de Avogadro. Incorporando una constante de proporcionalidad (R), donde el valor de R para una mol de cualquier gas se determina a partir de las condiciones ideales de un gas, como son:
PRESIÓN: 1 atm VOLUMEN: 22.4 L TEMPERATURA: 273 K Valor de R; R =1 atm x 22.4 L / 1mol x 273 K R = 0.082 atm L / mol K Quedando la ecuación de estado de la siguiente manera: |
Nemotecnia... para aprenderla o recordarla con facilidad::::
|
PV = nRT
Da clic sobre la imagen para ver la simulación de esta ley:
LEY DE DALTON O LEY DE LAS PRESIONES PARCIALES
|
“La presión total que ejerce una mezcla de gases en un recipiente es la suma de las presiones parciales de los gases presentes”.
Se formula así:
P. total = P1 + P2 + P3 + ... La mayoría de los gases son insolubles al agua, por lo que en el laboratorio se obtienen fácilmente con el método de desplazamiento del agua. Por tanto para calcular la presión del gas seco, es necesario conocer la presión del vapor de agua a esa temperatura.
|
La presión que ejerce un gas es proporcional al número de moléculas presentes en el gas, e independientemente de su naturaleza. En una mezcla gaseosa cada uno de los gases obedece la ecuación del gas ideal, por lo tanto, si todos los gases se encuentran en las mismas condiciones de volumen y temperatura, tenemos:
|