Las soluciones se clasifican principalmente bajo dos criterios, aunque hay autores que hablan de otras formas de clasificación. Aquí se hace referencia en: Según la cantidad de soluto
disuelto en relación con el solvente y según el tipo de solución de acuerdo al solvente que la conforma.
Soluciones según la concentración de soluto
¿Al mezclar dos sustancias el volumen aumenta?......Observa el vídeo! |
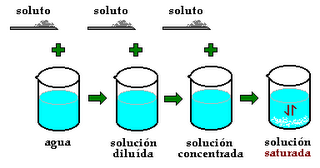
De acuerdo con la cantidad de soluto presente en una solución estas se clasifican en: insaturada o diluidas, saturada o concentrada y sobresaturada.
Diluidas o Insaturadas: Cuando contienen una pequeña cantidad de soluto, con respecto a la cantidad de solvente presente. Ejemplo: Si solamente disolvemos 8 g de X en 100 mL de agua, la solución es insaturada porque no hemos llegado a la cantidad máxima de soluto que podemos disolver. Saturadas o concentradas: Si la cantidad de soluto es la máxima que puede disolver el solvente a una temperatura dada. Ejemplo: Si la solubilidad de una sustancia X es de 10 g en 100 mL de agua. Esto significa que para preparar la solución saturada podemos disolver 10 g de la sustancia X en 100 mL de agua. Sobresaturadas: Este tipo de soluciones se consiguen cuando se logra disolver el soluto por encima de su punto de saturación por influencia del calor. Ejemplo: Si añadimos 13 g de X en 100 mL de agua, hemos sobrepasado la cantidad máxima de soluto que se puede disolver y parte de ese soluto quedará en el fondo del envase sin disolver, obteniendo una solución sobresaturada |
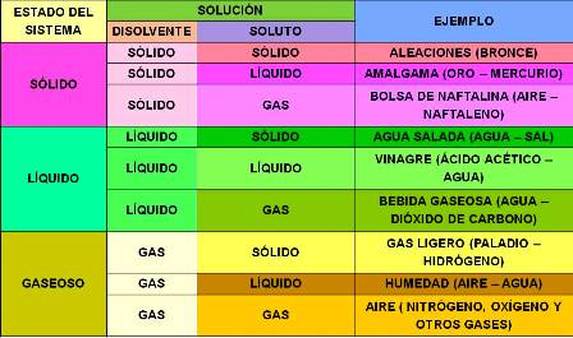
Según el estado de los componentes (solvente)
El solvente de las soluciones pueden ser el agua u otra sustancia como por ejemplo el benceno, tetracloruro de carbono, percloroetileno y acetona. Cuando el disolvente es agua se denominan soluciones acuosas.